| Auteur | Message |
|---|---|
|
Administrateur
|
291 éléments sur Terre, pendant que les théories en prédisent jusqu’à peut‑être 7 000 possibles. Mais où sont les atomes disparus ? Cette question, c’est le titre de la conférence de 2008, postée plus bas, dont je rapporte quelques notes clés, qui feront de bons rappels de la physique atomique de base (pas de chimie dans ce sujet).
Cette conférence parle de deux choses en parallèle : la nucléosynthèse et la recherche sur les atomes, avec le programme GANIL (Grand Accélérateur National d’Ions Lourds). La nucléosynthèse, c’est la synthèse — naturelle ou artificielle — des nucléides composés de nucléons, ce qui dans ce contexte, signifie la synthèse d’atomes caractérisés par leurs nombres de protons et de neutrons. La recherche sur les atomes, est toujours d’actualité, plus que ne le laisse paraître la vulgarisation scientifique et son besoin de spectacle, qui laisse croire à tord que la physique est dans une course au plus petit et qu’elle déprécie les niveaux supérieurs. Comme le dit une approche empirique des phénomènes complexes, nommée « systémique », à chaque niveau d’organisation des choses correspond une nature propre, qui ne peut pas vraiment se déduire de ses constituants, et il convient d’étudier également chaque niveau d’organisation pour lui‑même. C’est ainsi que le niveau d’organisation des atomes, est toujours un sujet d’étude d’intérêt — l’était encore au moins en 2008 et 2012‑2013 (et probablement encore maintenant). Mais où sont les atomes disparus ? — Conférence du CEA, à Caen Philippe Chomaz avec une collègue à lui (je ne sais pas son nom) Anecdote : le premier et principal intervenant, Philippe Chomaz aime beaucoup les vaches et est subjugué par le magnésium du yaourt, comme vous pourrez le découvrir au cours de cette conférence. Sa passion immodérée pour les vaches et l’inépuisable science qu’il a de celles Normandes en particulier, a fait l’objet d’un sujet spécifique : Les vaches normandes. Résumé sur GANIL et la nucléosynthèseÉléments, protons et neutrons (et isotopes)Les éléments sont caractérisés par leurs noyaux, eux‑même caractérisés par leurs nombre de protons. Les électrons intéressent surtout la chimie, généralement moins nucléosynthèse, et parfois quand‑même lorsqu’ils participent à une réaction dans les noyaux. Le noyaux des éléments est constitué de protons et de neutrons. Le nombre de protons est le nombre le plus caractéristique, et des éléments ayant le même nombre de protons, même s’ils ont un nombre différent de neutrons, auront typiquement le même nom. Les variantes d’un élément, qui varient par le nombre de neutrons, sont nommées « isotopes » de cet élément. On passe d’un élément à un autre en changeant le nombre de protons. Pour un élément donné, on passe d’un de ses isotopes à un autre, en changeant le nombre de neutrons. Il y a des contraintes à ces nombres, on ne peut pas créer un noyau avec un nombre de protons ou de neutrons arbitraire. Le proton a une charge électrique positive (et un spin). Le neutron n’a pas de charge électrique (ou a une charge neutre). Le neutron a une masse légèrement supérieure à celle du proton. Le neutron peut se désintégrer en proton, laissant s’échapper un électron et un anti‑neutrino. Un proton peut se désintégré en neutron, laissant s’échapper un positron (équivalent positif de l’électron) et un neutrino; un proton peut aussi muter en neutron, en captant un électron, et en émettant alors un neutrino, cette fois sans émettre de positron. Les protons, comme ils ont une charge électrique positive, se repoussent. La force nucléaire forte, agit à deux niveaux : à l’intérieur des neutrons et des protons en tenant ensemble les quarks qui les constituent, et, mais avec une distance limite, sur les neutrons et protons entre eux, les tenant ensemble dans le noyau. La portée (distance à laquelle elle peut agir) de la force nucléaire forte est beaucoup plus courte que la porté de la force électromagnétique (qui elle, est infinie, même si elle décroit vite avec la distance). La force nucléaire forte porte bien son nom : dans un noyau, un proton, qui est une chose très‑très‑très petite, est tenu par une force de plusieurs millier de tonnes qui l’empêche de s’échapper du noyau auquel il est lié. Un noyau ne peut pas capturer un nombre indéfini de neutrons et ne peut pas former n’importe quels isotopes, car au delà d’un certain nombre de neutrons (dépendant du nombre de protons), les neutrons n’interagissent plus, ne se lient plus avec le noyau, ne sont plus retenus par la force nucléaire forte. Est‑ce un effet liés à la taille du noyau et à la portée de la force nucléaire forte ? À vérifier… Éléments « naturels » et éléments « exotiques »On caractérise un élément, atome, par son nombre de protons et de neutrons, respectivement Z et N, la somme des deux indistincts, étant nommée « nombre de masse ». Le nombre de protons, Z, est plus important que le nombre de neutrons, N. C’est le nombre de protons, qui donne son nom à un atome, ses variations, variant par leurs nombres de neutrons, sont nommées des isotopes. Le nombre de neutrons est plus susceptible de changer que le nombre de protons, la variation du nombre de protons faisant intervenir une réactions plus complexe que la variation du nombre de neutron. On compte sur Terre, 291 éléments ou atomes. Ces 291 éléments sont en fait 80 éléments environ, correspondant à des nombres de protons, et leurs différents isotopes, correspondant chacun à différent nombre de neutrons. Dans ce contexte, on ne s’intéresse pas à la variation du nombre d’électrons, qui ne concerne pas la nucléosynthèse, mais la chimie. Ces 291 éléments ont un noyau stable, même si certains sont en réalité instable sur le long terme, comme l’uranium et le thorium, les principaux éléments radioactifs existant sur Terre sous forme de trace, et qui sont radioactifs précisément parce qu’ils se désintègrent, se transformant en d’autres éléments de nombre de protons moindre. Les protons et neutrons qu’ils perdent en se désintégrant, sont ce qui constitue le rayonnement radioactif. Ce rayonnement, c’est ce qu’ils laissent s’échapper en se muant en d’autres éléments plus simples (de nombre de masse plus faible). Sur Terre, la nucléosynthèse artificielle, a permis de créer environ 2 000 noyaux artificiels, synthétisés de depuis F. Joliot‑Curie. Là aussi, parmi ces 2 000 éléments, certains sont des variations isotopiques (des isotopes différents, variatons d’un élément canonique caractérisé par son nombre de protons). Dans l’Univers, les théories prédisent l’existence de 5 000 à 7 000 noyaux exotiques possibles, restant à synthétiser ou à découvrir. De 5 000 à 7 000, c’est une fourchette présentant une marge d’erreur de 40%, ce qui trahis un gros degré d’incertitude sur le nombre. Ce qui est exotique pour nous, est normal ailleurs dans l’Univers. Le caractère exotique d’un élément, d’un atome, est relatif. Processus de nucléosynthèseLa première nucléosynthèse, est celle ayant suivit le Big Bang. Elle a produit principalement de l’hydrogène (et de l’hélium ?). Dans les étoiles, pendant leur vie et même quand leur noyau implose (avant d’ensuite exploser et/ou se transformer en trou noir), sous la pression et par fusion nucléaire, des protons peuvent s’associer pour former des éléments plus lourds. À proximité d’une supernova émettant des neutrons, la matière environnante peut capter ces neutrons et muter en isotopes. Les neutrons de ces atomes peuvent aussi se désintégrer en protons, faisant muter le noyau en celui d’une autre élément. Les éléments instables se désintègrent le plus souvent rapidement et en quelques secondes, en éléments plus stables. D’autres éléments instables mais à désintégration lentes subsistent, et son ceux que l’on appel des éléments radioactifs. Tous les éléments sont instables, c’est seulement que ceux que l’on appellent stables, ont une durée de vie très longue, encore plus longue que celle des élément dits radioactifs. L’élément le plus stable, n’est pas le plus léger ni le plus simple : c’est le fer. Les atomes de fer sont difficiles à fusionner, et leur fusion consomment de l’énergie au lieu d’en libérer; les atomes de fer sont ceux dont la désintégration est la plus longue. Carte des noyaux dans « l’espace » neutrons × protons
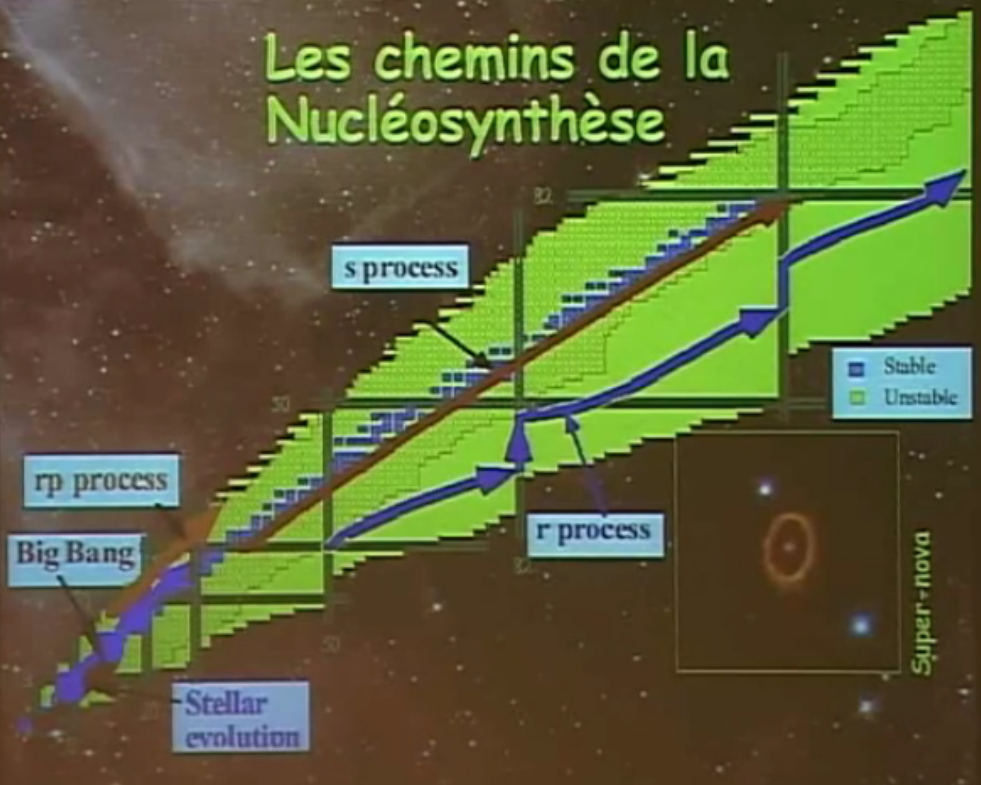 Même type de carte, avec des couleurs différentes. Sont ajouté des indications des conditions dans lesquels se produit la nucléosynthèse des éléments de cette carte.
 Des noyaux instables, créés par capture de neutrons, après un peu plus d’une seconde, se sont partiellement désintégré et s’approche des éléments stables. Pendant le processus, certains neutrons se transforment en protons.  Des noyaux instables, créés par capture de neutrons, après un peu plus de quatre secondes, se sont presque totalement désintégré et sont peu loin d’avoir muté en éléments stables. Pendant le processus, certains neutrons se transforment en protons. GANILLa conférence fait beaucoup de références aux accélérateurs GANIL et Spiral 2, et au détecteur INDRA, et parlent de leur avenir. Ce résumé n’en dira pas plus, et invite plutôt à visiter le site de ce programme, qui bien que situé en france, est Européen et international : ganil-spiral2.eu. |
|
Administrateur
|
Le résumé ci‑dessus ne rapporte pas fidèlement la conférence, il est est agrémenté d’additions qui ne sont pas explicitement marquées comme telles. Ces ajouts me semblaient nécessaires pour ne pas laisser de trous, et au moins, ç’aurait été dommage de les omettre.
|
|
Administrateur
|
Hibou a écrit : […] Ce qu’on peut lire entre ces lignes aussi, en étant pointilleux, c’est qu’un atome n’est pas à proprement parler, radioactif, car un atome isolé n’émet un paquet d’énergie qu’à l’instant où il se désintègre et devient un autre atome (qui pourra lui‑même ou pas être sujet au même processus). Un atome isolé, devrait plutôt être dit avoir une bonne probabilité de désintégration. Rigoureusement, on ne devrait parler d’élément radioactif, que pour des grandes quantité d’atomes ayant une bonne probabilité de désintégration (probabilité à l’échelle humaine). |
|
Administrateur
|
Hibou a écrit : Sur Terre, la nucléosynthèse artificielle, a permis de créer environ 2 000 noyaux artificiels, synthétisés de depuis F. Joliot‑Curie. […] Et quatre nouveaux venus ont été récemment baptisés par l’IUPAC (International Union of Pure and Applied Chemistry) : IUPAC is naming the four new elements Nihonium, Moscovium, Tennessine, and Oganesson (iupac.org), 8 Juin 2016. En plus d’un nom, ils ont reçu un symbole, comme pour tous les éléments. Leurs noms, symboles et numéros atomiques (somme du nombre de protons et du nombre de neutrons), sont :
Dans la vidéo ci‑dessous, un physicien dont le nom n’est pas indiqué (seul le nom de celui qui film est donné), parle de cet événement exceptionnel où quatre éléments ont été baptisés en une seule journée (c’est ça, qui est exceptionnel). Je l’écouterai et la résumerai plus tard. |
